[新しいコレクション] マグネシウム 原子量 高校 319394-マグネシウム 原子量 高校
高校生 約1年前 ゲスト ・57gの塩化マグネシウムMgCl2の物質量は何molか? ・また、これに含まれるMg2およびClの物質量はそれぞれ何molか?教えてください>< Mgの原子量は24、Clの原子量Nhk高校講座 化学基礎 第23回 化学反応式と量的関係 と、左辺と右辺で、原子の種類も数もまったく同じになっており、それぞれの物質につけた係数によって調節されています。 こうして求められたそれぞれの値を比較すると、マグネシウムの物質量とNhk高校講座 化学基礎 第19回 物質量 nhk高校講座 に、すべての物質はその原子量 で19gを割ると、塩化マグネシウム19gの物質量は0.molと
原子番号12番のマグネシウムには3種類の安定な同位体が存在しその割合はおよそ Yahoo 知恵袋
マグネシウム 原子量 高校
マグネシウム 原子量 高校-マグネシウムの栄養と働き、消化、吸収、マグネシウムが多い食品 マグネシウム (ラテン語 magnesium) は原子番号12の金属元素。 元素記号は Mg。 マグネシウムは周期表第2族元素の一種で、ヒトを含む動物や植物の代表的なミネラル(必須元素)であり、とりわけ植物の光合成に必要なFdData 高校入試:中学理科2 年:酸化・燃焼・還元 に激しく熱や光を出しながら燃える(酸素の量が多いから)。 この実験においてできた酸化鉄は,鉄の原子と酸素の原子が2:3 の割合で結び
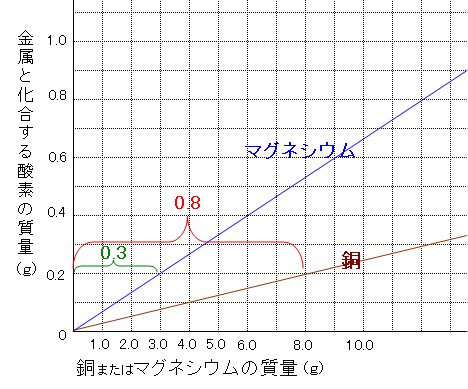



中学理科 銅とマグネシウム原子1個の質量比を求める なるほどの素
従って、マグネシウムも 0.1/22.4mol だけ必要です。 マグネシウムの原子量は24.3(1molが24.3g)ですので、必要なマグネシウムの質量は 24.3 × (0.1/22.4) = 0.108g ④マグネシウムリボン100cmはgとしてマグネシウムリボンは何cm必要か 比を用いて 1.00 : 0.0143 = x : 0.108 x = 7.552 ・・・ ≒ 7.55 cm レポートの書き方ですが、 ・ど プロ講師解説このページでは『高校化学で頻出の分子・化合物一覧』について解説しています。解説は高校化学・化学基礎を扱うウェブメディア『化学のグルメ』を通じて6年間大学受験に携わるプロの化学講師が執筆します。 炭酸マグネシウム MgCO 3問題 必要があれば,原子量および定数は次の値を使うこと。 原子やイオンの電子配置に関連する記述として 誤りを含むもの を,次の①~⑥のうちから一つ選べ。 ① ナトリウム原子のK殻には,2個の電子が入っている。 ② マグネシウム原子のM殻には,2
高校化学 中学化学 第1編 物質の状態 第1章 物質を構成する原子と分子 1 原子 物質 分子 化学式物質の マグネシウムに関する情報をまとめました。 基本情報 和名:マグネシウム 英名:Mgnesium 語源:ギリシャ語「マグネシア地方(Magnesia)」 元素記号:Mg 原子量:2431 常温(25℃)での状態:固体(金属) 色:銀白色 密度:1738 g/cm 3 (℃) 融点:650℃ 沸点:1095℃リチウム原子とナトリウム原子⑵ ナトリウム原子とマグネシウム原子 博 どちらが大きい? 原子の大小関係と比較の仕方|高校化学をスキマ時間でわかりやすく
65 Tb テルビウム 153 66 Dy ジスプロシウム 67 Ho ホルミウム 68 Er エルビウム 69 Tm ツリウム 163 70 Yb イッテルビウム 71 Lu ルテチウム原子量表10に基づく分子量計算 → 原子量表17を用いた場合は こちら 分子式(C6452H9926N1714O40S54等)を入力し,「分子量」を押してください. 分子式: 水和物や塩など,2分子以上の合計分子量を計算したい場合はそのまま続けて入力してくださいマグネシウムMgについて マグネシウムは第2族元素ですが、ベリリウムと同様にアルカリ土類金属ではありません。 炎色反応を示さず、塩基性も弱いためです。 単体は銀白色の金属で、火をつけると強い光を発しながら燃えます。




を教えてください を教えてください 高校 教えて Goo




高校化学 計算問題 まとめページ 井出進学塾 富士宮市の学習塾 井出進学塾 マンツーマンの個別指導の専門塾
Start studying 高校化学基礎/覚えておきたい原子量・分子量・式量 Learn vocabulary, terms, and more with flashcards, games, and other study tools有望な物質であるマグネシウム もう一つ、埋蔵量の問題があります。先ほど100億tの石炭に代わるものという話をしまし たが、例えば亜鉛を使うという提案もいくらでもあります。しかし亜鉛の世界の埋蔵量は4億 tぐらいしかありません。(5)次に,このMg(原子量 Mg=243)の質量が何gに相当するか。有効数字3桁で求めます。 (6)マグネシウムリボン10(cm)の質量は( )gです。(5)で求めた質量が何(cm)になるか計算しま



2




高校化学基礎の質問です 写真 から は解けました はどのような考え 化学 教えて Goo
Mg2HCl→MgCl 2 H 2 (2)は、物質の 過不足 に関する問題です。 問題文から原子量24のマグネシウムが24g存在するということがわかっています。 つまり、マグネシウムは1mol存在しているわけですね。 一方、塩酸は 「十分な量」 と書かれていますね。 ということは、 マグネシウムはすべて反応した ことになります。 ですからこの場合は、係数の比の通りに、H 2 も1mol発生します。 よって、 見本高校理科地歴コース 本科 化学基礎 要点学習見本高校コース 本科 化学基礎 要点学習qcs5a1z1j5 イオンとその生成 陽イオン:原子が電子を放出してできる,正の電荷をもった粒子。結晶格子の密度と原子量や質量などの値を求める計算問題の解き方です。 結晶格子の計算問題が難し分子量というのは分子内の原子量の和 マグネシウム(元素記号Mg,原子番号12)の特性について解 に原子量の変動範囲₁₀₀₇₈₄~₁₀₀₈₁₁,次に「原子量表(₂₀₁₀)」の値₁₀₀₇₉₄±₀₀₀₀₀₇が示されており,その下に




イオン化傾向 イオン化列 と反応性 金属の酸化還元




質量 1kg 重力 重さ 9 8n 重力加速度 地球の重力によって生じる加速度を重力加速度 通 常は 記号 G を用いて表す と呼ぶ 高校物理のレベル では 一定の値とし 9 8m S 2 を用いる 中学校理科の レベルでは 重力加速度を直接的に問題にすることは ないが
マグネシウム 原子量 原子の質量を表す数値である。 炭素原子の質量を12として、これを基準にそれに対する比でそれぞれの原子の質量を表したもの。 また、練習問題も基本的なものから入試レベルまで幅広く掲載し、日常の学習から高校受験まで化合物の原子量表 (元素の原子量は,質量数12の炭素( 12 C)を12とし,これに対する相対値とする。 但し,この 12 C は核および電子が基底状態にある結合していない中性原子を示す。 ) 多くの元素の原子量は通常の物質中の同位体存在度の変動に化学 物質量の求め方 次の計算の仕方と答えを教えてください! 1水素原子 24×10の24乗個の質量 2ナトリウムイオン60×10の22乗個の質量 3マグネシウム原子1個の質量 質問No



2




酸化還元反応 電子のやり取り
©₂₀₂₁日本化学会 原子量専門委員会 原 子 量 表 (₂₀₂₁) (元素の原子量は,質量数₁₂の炭素( 12c)を₁₂とし,これに対する相対値とする。但し,この 12cは核および電子が基底状態にある結合してい ない中性原子を示す。「原子量・分子量・式量」とモル質量との違い 物質量(モル:mol)とアボガドロ数の違いや関係は? 計算問題を解いてみよう コロイドの性質 チンダル現象・ブラウン運動・電気泳動とは? クメン法とは分子量というのは分子内の原子量の和のことです。しかしながら、アルミニウムの単体は分子を作りませんのでアルミニウムは原子量で計算を行います。 問題 マグネシウム原子1個の質量を求めよ 30万冊を超える大学生、高校生、中学生のノートを
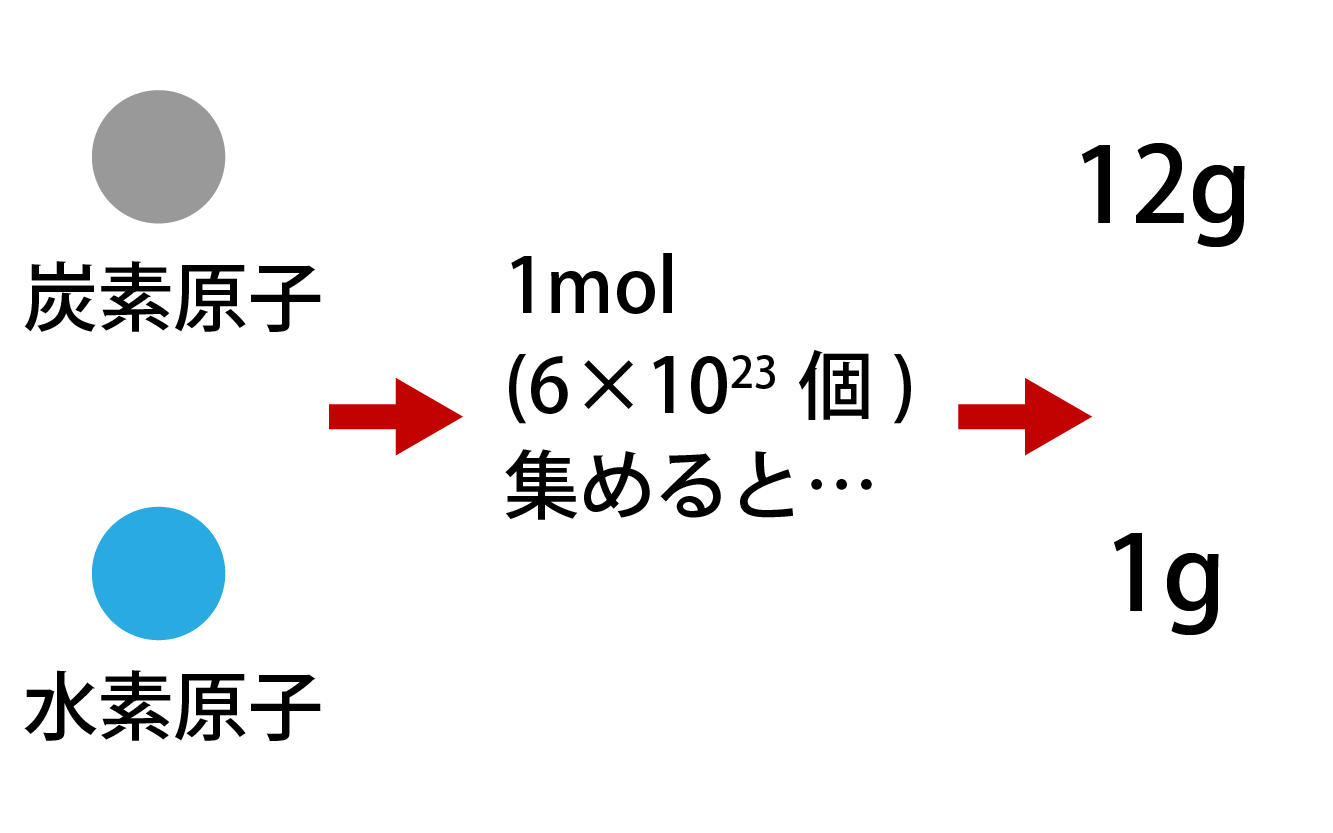



原子量とは 求め方や単位も見やすい図と例で即理解 分子量との違いも 高校生向け受験応援メディア 受験のミカタ




新編化学基礎 令和4年度用高等学校教科書 シラバス 東京書籍
マグネシウムは実用金属の中で最も軽く、多くの優れた性質を兼ね備えます。板材,マグネシウムの購入は、金属材料カット通販・販売のEMetalsまで! マグネシウム マグネシウム 原子量百科事典マイペディア 「マグネシウム」の解説 マグネシウム 元素記号 はMg。 原子番号12,原子量〜。 融点650℃,沸点1095℃。 アルカリ土類 金属元素 の一つ。 古くからその存在は知られていたが,1808年デービーが初めて金属を分離。 銀白色の金属。 軽金属に属する。 空気中では表面は酸化マグネシウムの被膜におおわれる。 空気中で強く熱すると閃 (せん)光を放って燃え©₂₀₁₅日本化学会 原子量専門委員会 原 子 量 表 (₂₀₁₅) (元素の原子量は,質量数₁₂の炭素( 12c)を₁₂とし,これに対する相対値とする。但し,この 12cは核および電子が基底状態にある結合してい ない中性原子を示す。




高校 一年 化学 質問です 前回 テストで指数計算を行ったら周りの数 化学 教えて Goo
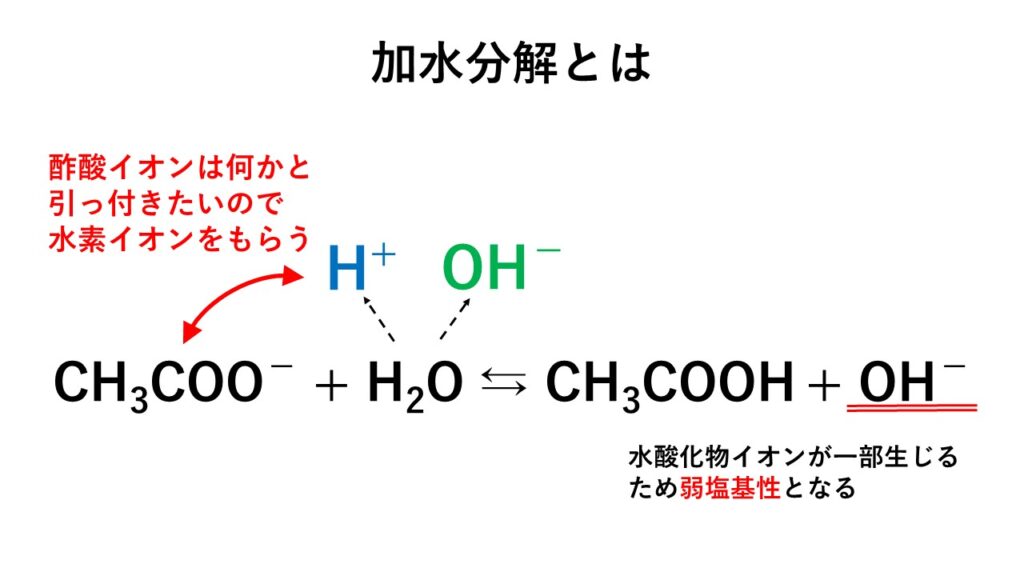



5分でわかる 塩の加水分解と塩の種類と分類 液性を解説 サイエンスストック 高校化学をアニメーションで理解する




新品 完全未使用 新品 高校化学 教科書 数研出版 化学 文部科学省検定済 1冊 の落札情報詳細 ヤフオク落札価格情報 オークフリー スマートフォン版




中学理科 銅とマグネシウム原子1個の質量比を求める なるほどの素




周期表と覚え方 原子量 語呂合わせ 理系ラボ



化学基礎 物質の変化02 原子量の求め方 8分 Youtube




この問題の解き方を教えていただきたいです Clearnote




高校1年生です 化学で原子量を求める問題です 問題 ある金属mの その他 教育 科学 学問 教えて Goo



高校1年生の化学基礎なのですが解答と解説及び途中計算をお願いしま Yahoo 知恵袋




化学基礎 実教出版 高校教科書 メルカリ




57gの塩化マグネシウムmgcl2の物質量は何molか Clearnote



高校理科化学の質問です これなんで0 5molじゃなくて Yahoo 知恵袋



中2化学 原子1個の質量 中学理科 ポイントまとめと整理



Kondo Yuhei Com




化学 富士宮教材開発 井出進学塾




高等学校化学i 物質と原子 Wikibooks
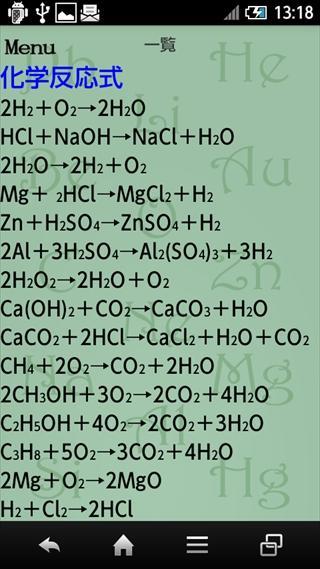



基礎化学式 中学や高校で学ぶ化学の基礎知識を手に入れよう Para Android Apk Baixar



メディアラボ株式会社 Gperiodic




問題 マグネシウム原子1個の質量を求めよ Clearnote




最新 中身も確認 高校化学を学ぶおすすめ本 社会人からでも 受験生基礎にも最適 Next Topic



1




物質の状態 体積 密度 モル 0から始める高校化学まとめ Novita 勉強法



2




Mol 物質量モル と質量 高校化学 物質量 6 Youtube




高校化学 問題の答えは1番ですが 2 6の縦軸はそれぞれなにを表してい 化学 教えて Goo



中2化学 原子1個の質量 中学理科 ポイントまとめと整理



高校化学基礎の問題です 数研出版99ページ 原子量 分子量 物質量の問題で Yahoo 知恵袋




結晶格子 単位格子 の計算問題 アボガドロ定数や密度や原子量の求め方




文系化学基礎 2学期中間試験問題とその結果 高校化学の教材 分子と結晶模型の ベンゼン屋 楽天ブログ




高校化学 計算問題 まとめページ 井出進学塾 富士宮市の学習塾 井出進学塾 マンツーマンの個別指導の専門塾




銅の原子一個はマグネシウム原子1個の何倍か 原子の質量比 高校入試必出問題 Youtube



2




高校理論化学 Lite By Akio Terada




物質量は 0 2molと考えたのですが Ca2 とcl の合計が何molか分 Clearnote



化学のワークで式量を求めたいのですが 1 と 4 のダ Yahoo 知恵袋
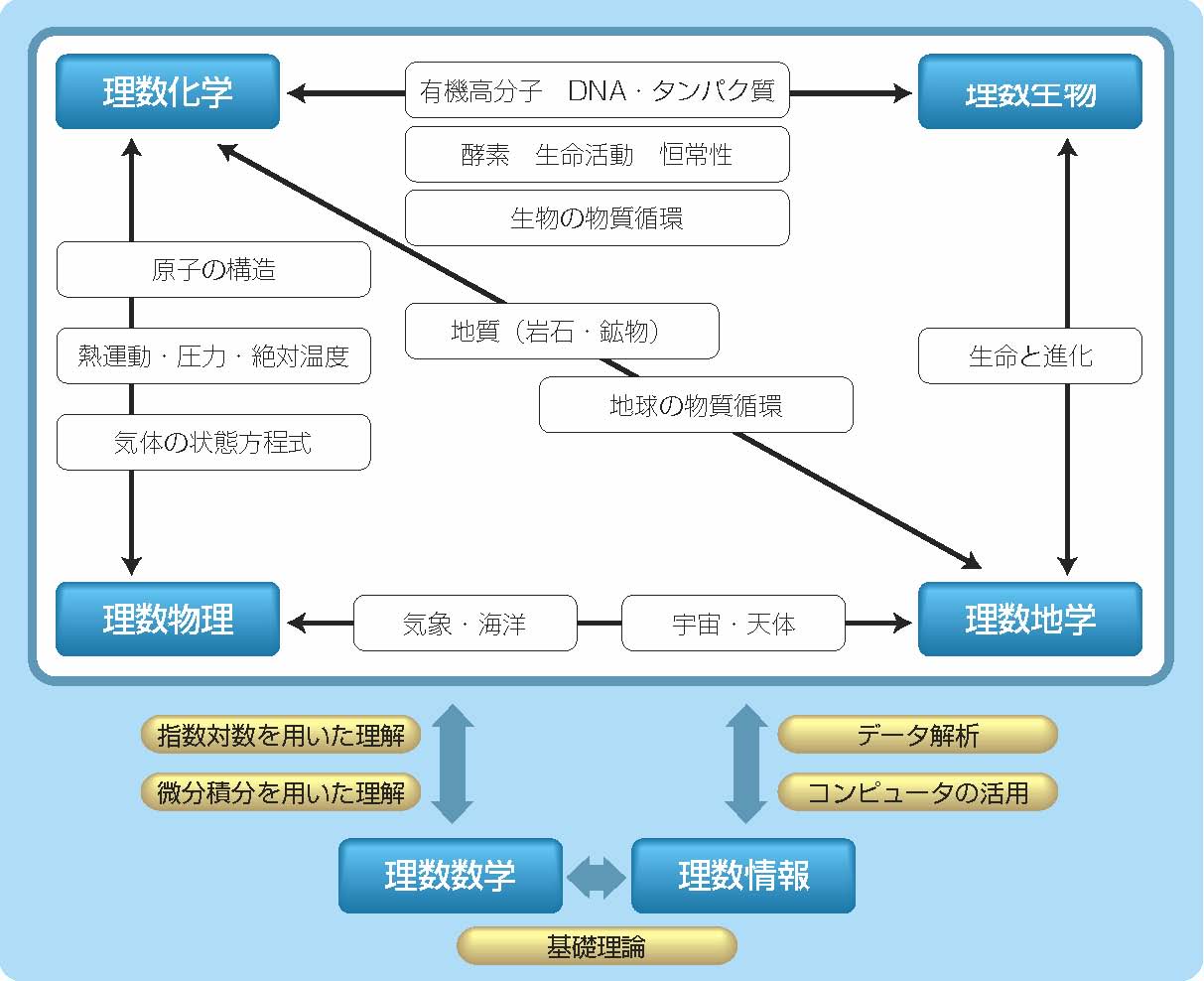



理数科 横浜サイエンスフロンティア高等学校




化学 教科書 数研出版 高校 教材 メルカリ
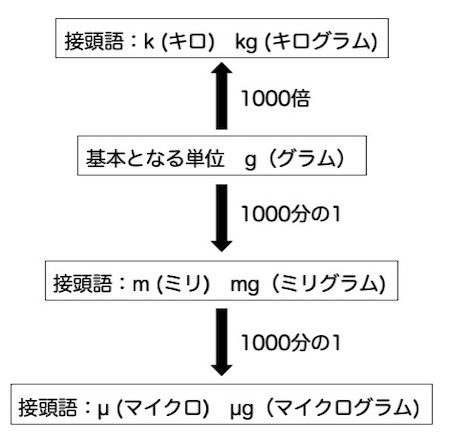



基礎から始める 単位の変換とモル計算の勉強法 Novita 勉強法




11 Nhk高校講座番組表 15 Pdf 4 5mb Manualzz
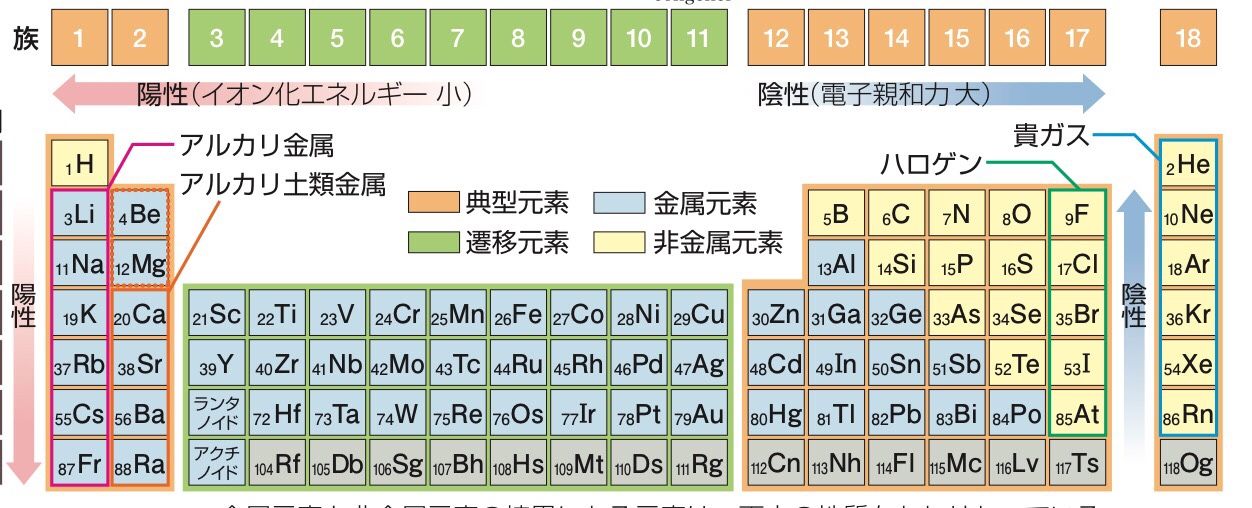



元素 ってなに 高校化学の教材 分子と結晶模型の ベンゼン屋 楽天ブログ




中身 使い方 高校の化学 が一冊でまるごとわかる レビュー Next Topic




中学2 3年理科の化学計算 ゴロ合わせで化学を楽々制覇 その 原子量 水の電気分解 金属の酸化と燃焼 Studygeek スタディーギーク




京大生が書いた高校化学基礎編 有効数字の見方 や 化学式の書き方 からはじめる I O Books Amazon Com Books



原子番号12番のマグネシウムには3種類の安定な同位体が存在しその割合はおよそ Yahoo 知恵袋




質量や原子数分子数と物質量 Mol を変換する計算問題




高校化学基礎 化学反応と過不足の計算 練習編 映像授業のtry It トライイット



3




高校理論化学 イオンの生成 イオン半径 イオン化エネルギーと電子親和力 受験の月
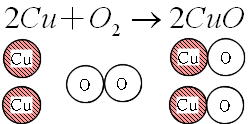



Science 化学変化と質量比 定比例の法則と原子量 分子量 働きアリ




高校化学基礎 過不足の計算1 映像授業のtry It トライイット
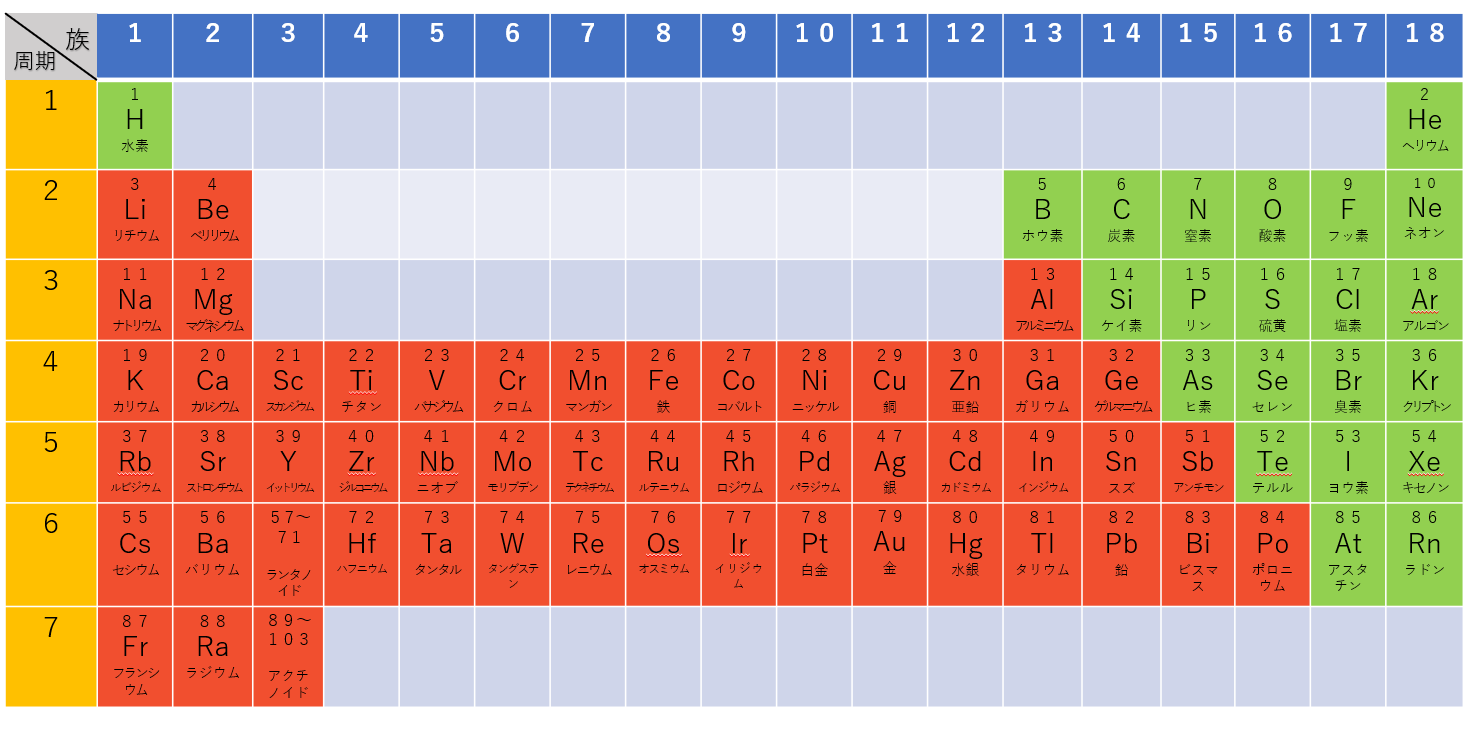



周期表と覚え方 原子量 語呂合わせ 理系ラボ




ヤフオク C 01 化学精義 竹林保次 培風館 昭和48年1月3
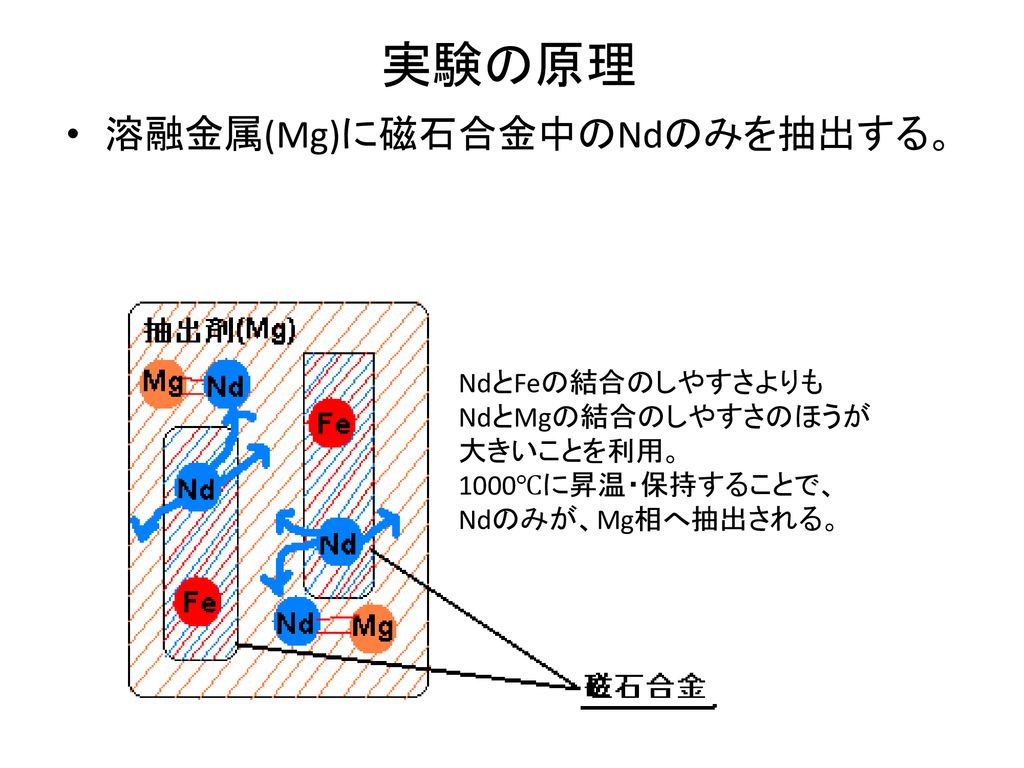



希土類磁石からのネオジムの回収 巣鴨高校2年 西村啓吾 Ppt Download
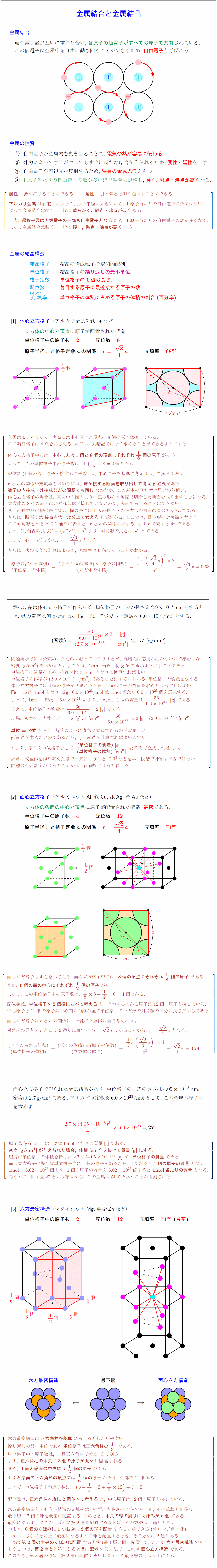



高校理論化学 金属結合 金属の性質 金属結晶 体心立方格子 面心立方格子 六方最密構造 受験の月




高校化学基礎 イオン化傾向と金属単体の反応性 映像授業のtry It トライイット




書籍情報 京大生が書いた高校化学 基礎編




考え方のところに書いてある 塩化マグネシウムの粒子の数は Mgcl2 Mg2 Clearnote




化学の組成式決定の問題です なぜ質量百分率を原子量で割れば原子の比 高校 教えて Goo




高校物理発想法 著者 大阪堺市周辺で高校物理 化学の家庭教師を行っております Pchometeacher Twitter
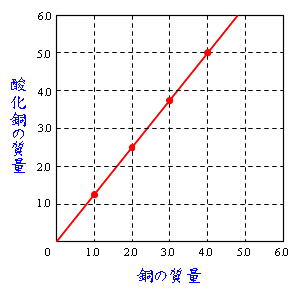



Science 化学変化と質量比 定比例の法則と原子量 分子量 働きアリ




無料学習動画 高校化学 Kawajiri Planning オンライン家庭教師




中学理科 銅とマグネシウム原子1個の質量比を求める なるほどの素



Kondo Yuhei Com




1 2 金属結晶の構造 おのれー Note



1




Nekomin Rikaさんのイラストまとめ




高校理論化学 Lite By Akio Terada




イオン化エネルギー徹底解説 周期表での法則も解説 受験スタイル




高校化学基礎 金属の反応性 練習編 映像授業のtry It トライイット




マグネシウム 元素記号mg 原子番号12 の特性について解説



高校化学 基礎 99番の 1 についてなんですけど まずm Yahoo 知恵袋



高校化学の基礎 内容を見る チャート式の数研出版




Nekomin Rikaさんのイラストまとめ




高等学校理科用 化学 数研出版 メルカリ
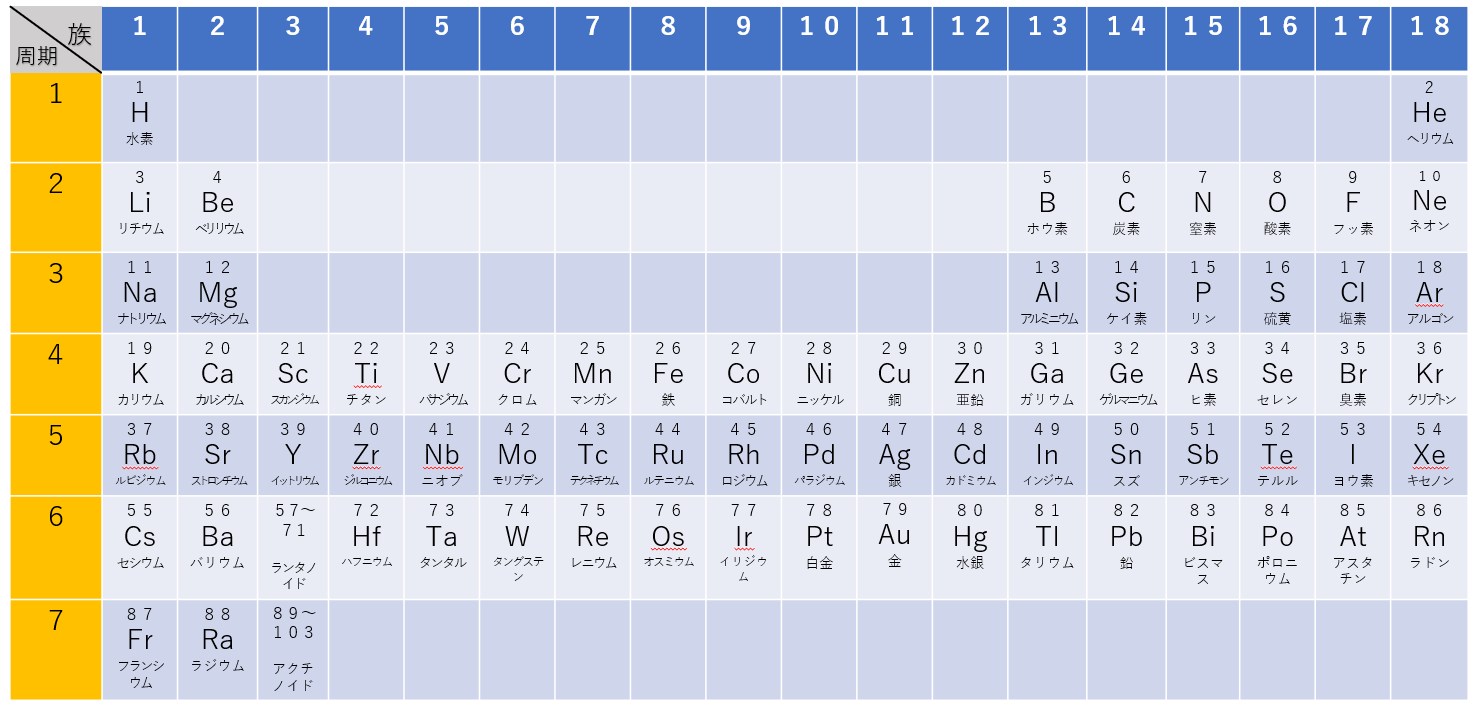



周期表と覚え方 原子量 語呂合わせ 理系ラボ




無料ダウンロード 高校 化学 組成式 一覧 高校 化学 組成式 一覧




基礎化学式 中学や高校で学ぶ化学の基礎知識を手に入れようのアプリ情報 予約トップ10
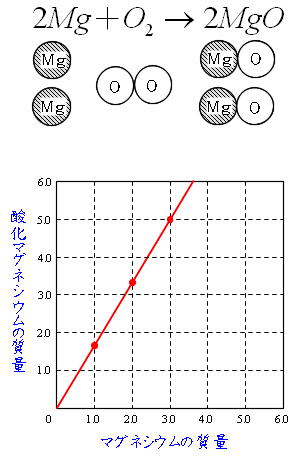



Science 化学変化と質量比 定比例の法則と原子量 分子量 働きアリ



3




この問題の解き方を教えていただきたいです Clearnote




高校化学基礎 ダースと本数 映像授業のtry It トライイット
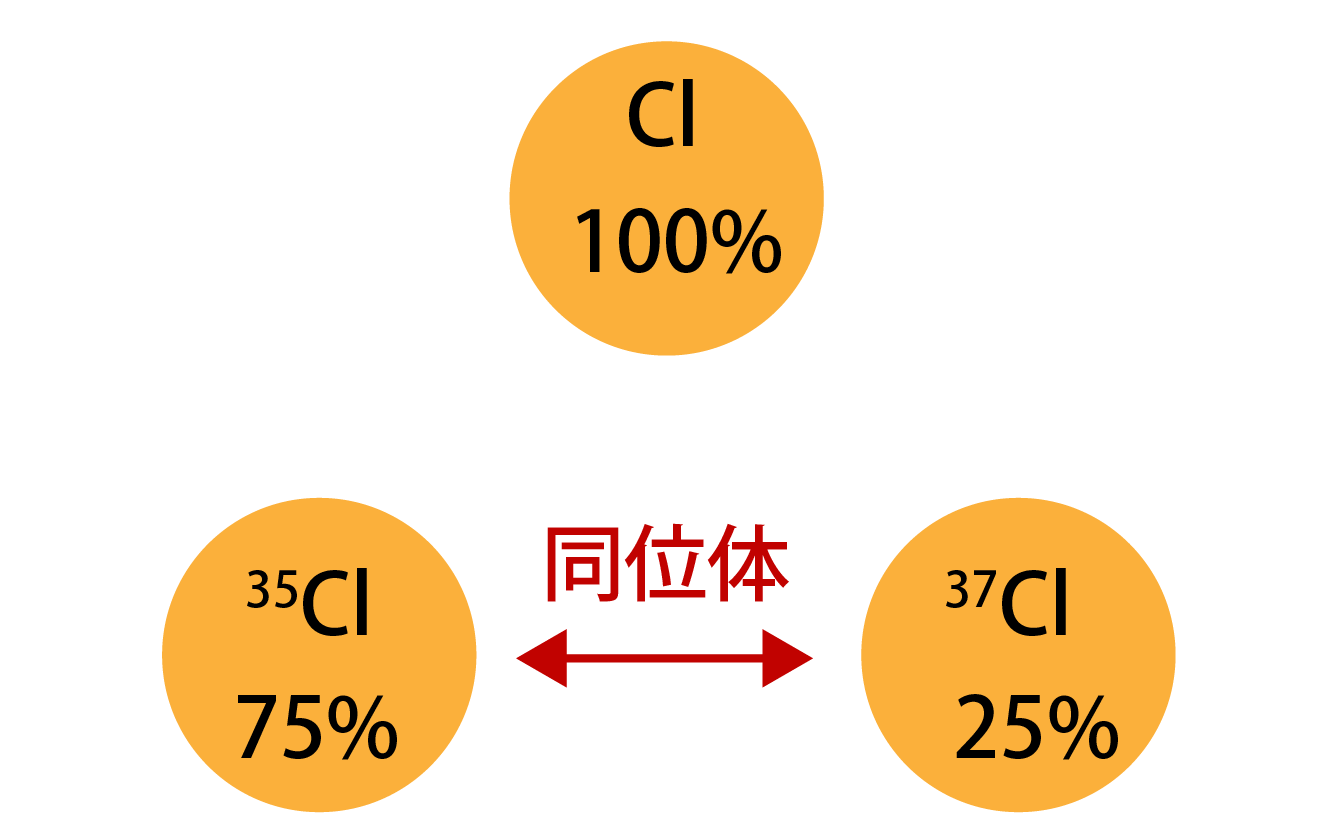



原子量とは 求め方や単位も見やすい図と例で即理解 分子量との違いも 高校生向け受験応援メディア 受験のミカタ




銅の原子一個はマグネシウム原子1個の何倍か 原子の質量比 高校入試必出問題 Youtube



こんにちわ 気体の塩化マグネシウムはmgcl2として存在する マグネシウムの Yahoo 知恵袋




この2題がどうしたらいいのかよく分かりません どなたか教えてください Clearnote




高校 新演習 スタンダード 化学 問題集 メルカリ




銅の原子一個はマグネシウム原子1個の何倍か 原子の質量比 高校入試必出問題 Youtube




中身 使い方 Newton別冊 学びなおし中学 高校化学 改訂第2版 ニュートン別冊 レビュー Next Topic




高校化学基礎 金属のイオン化傾向とは 映像授業のtry It トライイット
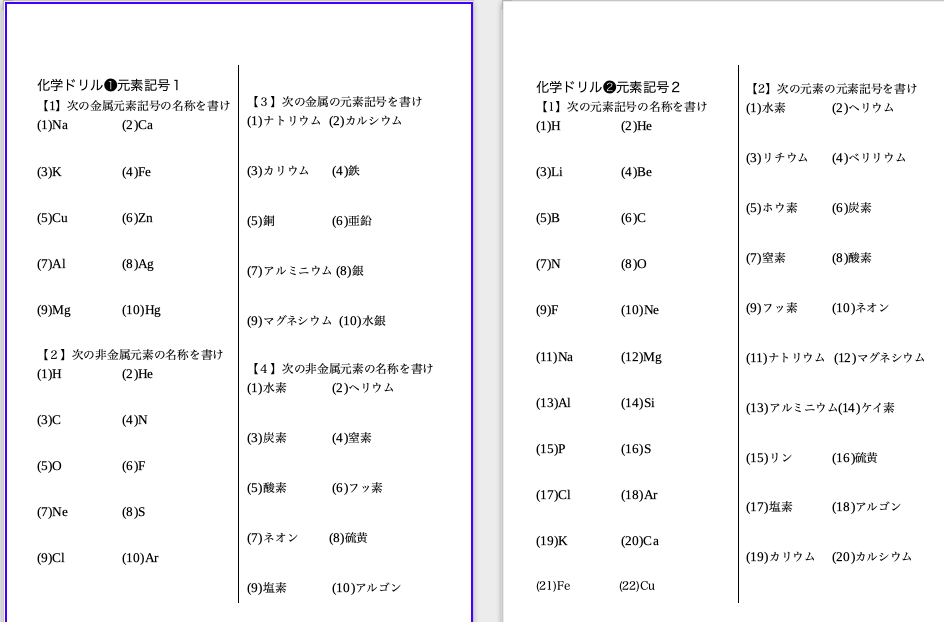



9ページ目の 授業 高校化学の教材 分子と結晶模型の ベンゼン屋 楽天ブログ
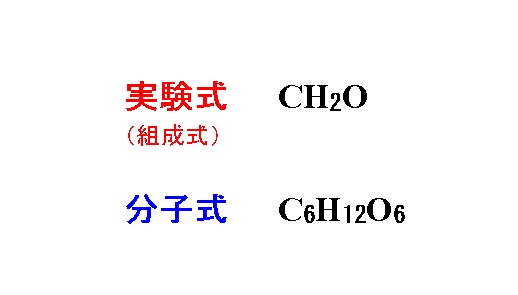



有機化合物の実験式 組成式 を求める計算と分子式の決定




Nekomin Rikaさんのイラストまとめ




周期表 Wikipedia




高校生物 見かけの光合成速度のグラフと物質量計算の問題の解き方 高校生物の学び舎
コメント
コメントを投稿